
花火の色は、もともとの火薬の色ではなく、花火師が火薬に着色料を細工することでつけられています。
<着色料>
花火に色を着けるために火薬に混ぜられる物質のことです。炎色反応を利用しています。
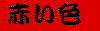
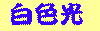






過塩素酸カリウム、過塩素酸アンモニウムなどと、アルミニウム(Al)、マグネシウム(Mg)の微粉末とを混ぜて高温火炎を作ると、白色に輝きます。
花火の他に、照明弾や船舶救難信号などに使用されます。

ナトリウム化合物が使われます。ナトリウム化合物は種類が多く、何でも使えますが、 シュウ酸ナトリウム、
氷晶石、ウルトラマリンなどが使われます。
食塩(NaCl)は湿気に弱いので使えません。

このときの発光分子は2原子分子であり、505〜535nmの帯スペクトルで緑の色を出します。
したがって、緑色の光を出すには 塩化バリウムを生成する必要があるため、塩素化合物が一緒に用いられます。

青い炎は、花火では昔から最も難しい色とされてきました。まだきれいな青は成功していません。
青い炎は銅の化合物によるものが多く、2原子分子 塩化銅の420〜460nmの部分が青の発光として最も良いのですが、これは比較的低温(〜1200℃)で鮮やかであり、高温になると他の部分の光によって青が弱められる欠点があります。

 最近はだんだんきれいな紫の色が出せるようになってきました。
最近はだんだんきれいな紫の色が出せるようになってきました。

炎色反応 | 身の回りの化学
このページの著作権は,木原 寛と今福京子が保有しています。







 花火の化学のページへもどる
花火の化学のページへもどる